Le speranze riposte nel vaccino russo Sputnik sembrano interrompersi già. Il Brasile non lo approva. Il virologo Roberto Burioni fa sapere – su Twitter – che i campioni analizzati in Brasile contengono virus in grado di replicarsi, con grandi rischi per la salute.
LA TECNOLOGIA DI SPUTNIK V E IL RIFIUTO DI ANVISA IN BRASILE
La mancata approvazione di Sputnik da parte di Anvisa, autorità sanitaria brasiliana, deriverebbe da alcuni dubbi sul ciclo di produzione dei vaccini in Russia – dove non verrebbero osservati gli standard di sicurezza – e dalla mancanza di una documentazione necessaria per il via libera. Ma non solo.
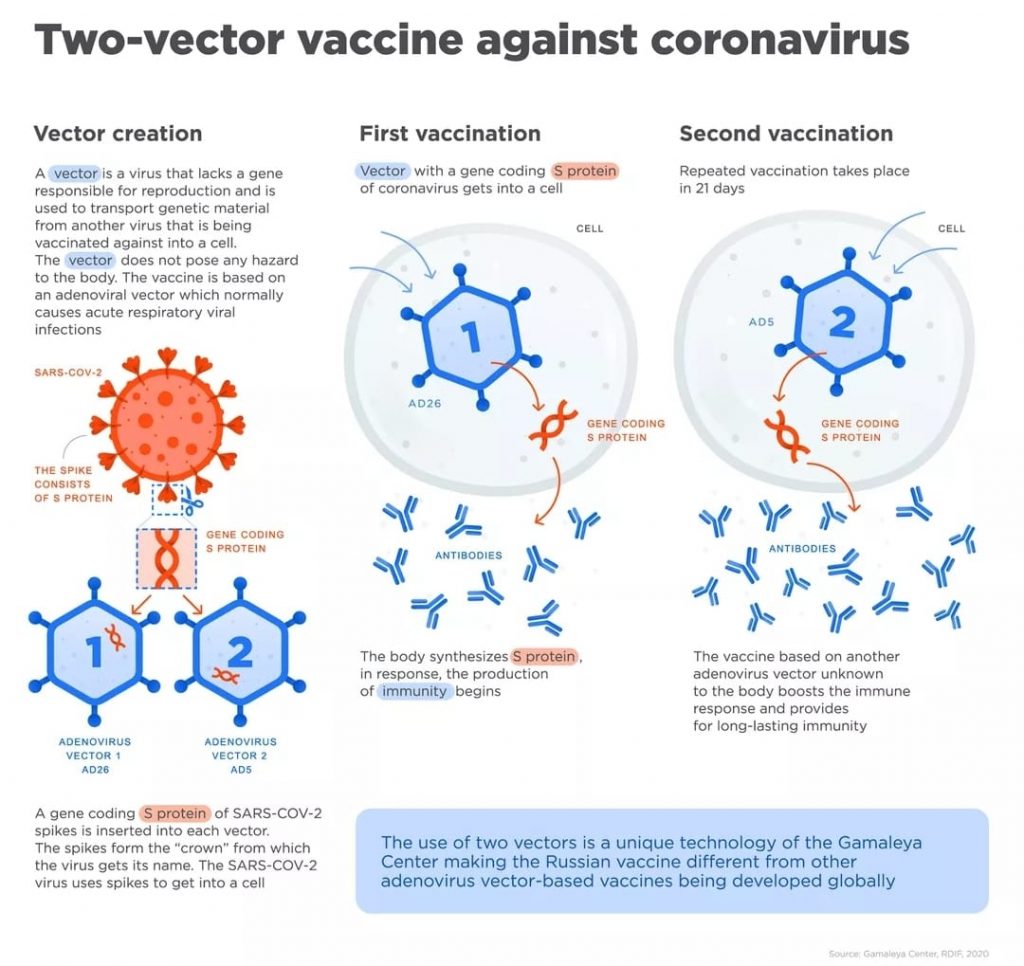
Sputnik V è un vaccino a vattore virale adenovirus che sfrutta una tecnologia tale da stimolare le cellule dell’organismo a cui viene iniettato a produrre una risposta immunitaria nei confronti di Sars-Cov-2. Ma stando alle analisi sulle fiale inviate in Brasile, anziché essere “nutralizzato”, l’adenovirus utilizzato sarebbe in grado di replicarsi e di causare raffreddori, gastroenteriti e altre complicazioni.
Così come il vaccino J&J, la prima dose di Sputnik utilizza un adenovirus umano, l’Ad26, la seconda invece l’Ad5. Per evitare la replicazione del virus e l’interazione con il sistema immunitario, vengono eliminati i geni Adv E1 ed E3. Se l’Adv E1 viene eliminato, il virus non può replicarsi e diventa “inattivato”. I virus inattivati dei vaccini risultano non pericolosi ma ugualmente efficaci nella prevenzione della malattia.
LO STUDIO SU THE LANCET
Tuttavia le dosi arrivate in Brasile – se fossero confermati questi dati – sembrerebbero contenere il virus attivo. Una circostanza mai verificata in quelle precedenti, i cui studi di fase 3 sono stati pure pubblicati sulla rivista scientifica The Lancet.
Nell’analisi di efficacia dello studio clinico di fase 3 randomizzato, in doppio cieco, controllato con placebo, sui 19.866 volontari coinvolti nell’analisi di efficacia, 14.964 hanno ricevuto il vaccino e 4.902 il placebo.
Il trattamento a due dosi di Sputnik V, somministrato a 21 giorni di distanza avrebbe dimostrato un’efficacia del 91,6% contro il coronavirus. Questo da un calcolo sull’analisi di 78 casi confermati di Covid-19 identificati nel gruppo placebo (62 casi) e nel gruppo dei volontari vaccinati (16 casi).
Gli effetti collaterali anche gravi sono stati rari sia nel gruppo placebo (0,4 [23/5.435]) che nel gruppo dei vaccinati (0,2% [45/16.427]), ma nessuno di questi è stato considerato associato alla vaccinazione, così come i 4 decessi verificatisi.
Gli eventi avversi riportati sono invece stati di scarsa entità e hanno incluso sintomi simil-influenzali, dolore nella zona d’iniezione e stanchezza.
Finora il vaccino russo è stato approvato in 60 Paesi nel mondo. Il Fondo russo per gli investimenti diretti in Russia ha criticato duramente la scelta di Anvisa. L’Ema sta attualmente dialogando con le autorità competenti russe dopo lo scorso sopralluogo in alcune cliniche.